近日,上海科技大学物质学院杨晓瑜课题组在叔醇和α-叔胺动力学拆分领域取得系列进展,相关工作分别以“Asymmetric Enamide-Imine Tautomerism in the Kinetic Resolution of Tertiary Alcohols”和“Kinetic Resolution of α-Tertiary Propargylic Amines through Asymmetric Remote Aminations of Anilines”为题发表于国际权威学术期刊《德国应用化学》(Angewandte Chemie International Edition)和美国化学会旗下催化领域旗舰期刊ACS Catalysis。
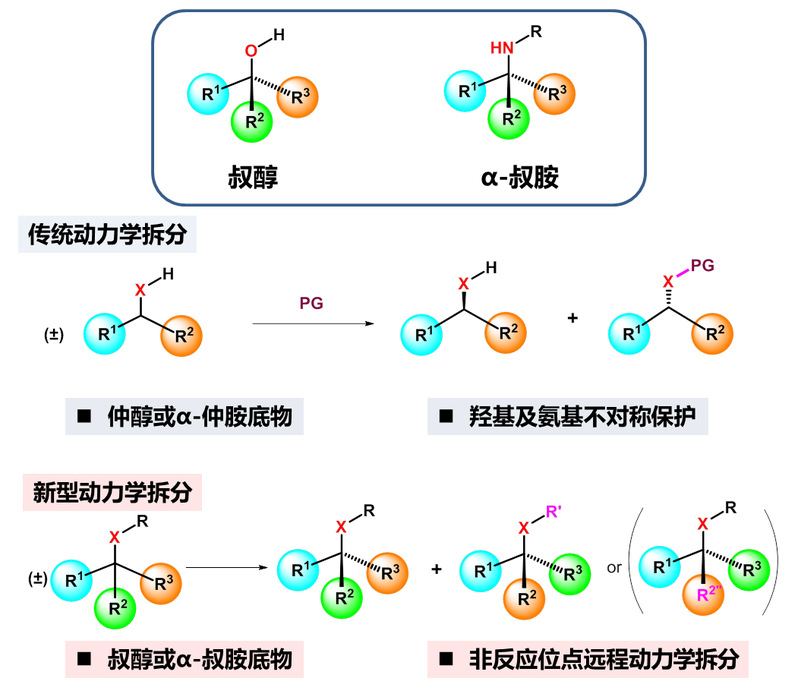
图 | 手性叔醇和α-叔胺以及传统动力学拆分方法
在第一项工作中,烯胺-亚胺的互变异构是有机化学中常见的一种异构化过程,由于烯胺-亚胺互变异构较低的能量需求,该过程往往被认为是极度可逆的,并且广泛存在于一系列有机反应的机理中,特别是不对称有机胺催化之中。在前期利用不对称分子内环化反应实现2-氨基烯丙基叔醇和2-氨基苄叔醇动力学拆分的基础上,杨晓瑜课题组通过手性磷酸催化的不对称可控烯胺-亚胺互变异构反应实现了烯丙基叔醇的动力学拆分反应,该方法对于二烷基取代烯丙基叔醇尤为有效。研究人员通过利用一个动力学拆分反应的产物即能实现β-氨基叔醇四个立体异构体的立体发散式合成的例子证明了该反应的应用潜力。杨晓瑜课题组2020级博士研究生唐梦瑶为论文第一作者,2017级本科生谷欢潮为第二作者。上海科技大学为论文第一完成单位,杨晓瑜教授为论文通讯作者。
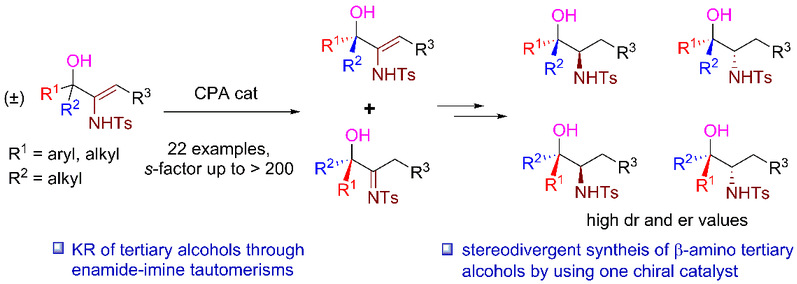
图 | 手性磷酸催化烯胺-亚胺不对称互变异构实现烯丙基叔醇动力学拆分
在第二项工作中,手性炔丙胺是一类重要的手性合成砌块,被广泛应用于手性药物和具有生理活性的天然产物的合成中。然而,目前对于α-叔炔丙胺(含有一个四取代手性中心的炔丙胺)的不对称合成方法仍然具有很大的挑战性。在已有的报道中,通过对酮亚胺的不对称加成反应是合成α-叔炔丙胺的一类有效的方法,然而该方法局限于活泼的酮亚胺底物 (酮亚胺α-位具有吸电子活化基团),而对于非活化酮亚胺的不对称炔丙基化反应则困难的多,之前仅有一例相关报告,但也仅获得了中等的对映选择性。在之前研究中,杨晓瑜课题组利用手性磷酸催化氢化喹啉和偶氮二甲酸酯的不对称芳香亲电胺化反应实现α,α-二取代氢化喹啉高效动力学拆分。
在此研究基础上,该团队近期又利用该策略应用于更具挑战性的非环状α-叔胺,首次成功利用手性磷酸催化苯胺和偶氮二甲酸二苄酯的不对称远程胺化反应首次实现了α-炔基叔胺的动力学拆分。该方法有着优异的底物适用性和出色的动力学拆分效果,并且α-氰基取代α-叔胺 (Strecker 反应产物) 在此条件下也能获得出色的拆分效果。克级规模实验以及对手性产物和原料丰富的衍生化反应也证明了该动力学拆分方法在合成手性α-叔胺类化合物中的实用性。杨晓瑜课题组2017级联合培养研究生潘永凯和2018级博士研究生王东磊为论文共同第一作者,上海科技大学为论文第一完成单位,杨晓瑜教授为论文通讯作者。以上工作都得到国家自然科学基金委和上海科技大学启动资金的支持。
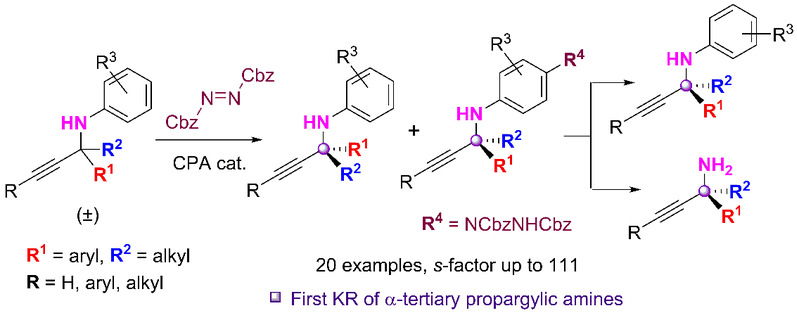
图 | 不对称远程胺化反应实现α-叔炔丙胺动力学拆分
论文链接:
https://onlinelibrary.wiley.com/doi/10.1002/anie.202106151
https://pubs.acs.org/doi/10.1021/acscatal.1c02331


