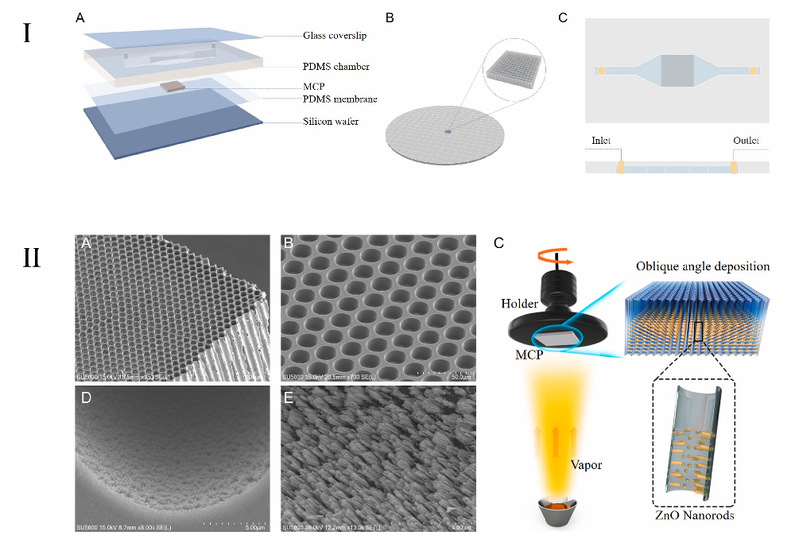
图1 I:(A)荧光增强数字PCR芯片分解示意图,(B)将微通道板(MCP)分割为4 × 4 mm2大小的区域,每个区域包含2.5 × 104个微孔,(C)荧光增强数字PCR芯片示意图的俯视图和横截面图。II:(A)扫描电子显微镜下微通道板(MCP)截面斜视图,(B)扫描电子显微镜下微通道板(MCP)截面的表面特写,(C)通过局部斜角沉积(LOAD)将ZnO纳米棒均匀地积淀在微通道板侧壁,(D)ZnO纳米棒功能化的微通道板上微孔的扫描电子显微图,(E)II(D)的局部结构放大图。
为增强dPCR临场快速核酸检测能力,刘一凡组与浙江大学研究团队合作开发出了一种基于ZnO纳米棒修饰的微通道板(MCP)集成dPCR微芯片(图1)。MCP是一种高度多孔的玻璃薄膜,通常用于实现检测中的粒子倍增。研究团队将MCP巧妙地集成在微流体芯片中,为PCR反应体系提供海量独立的微腔室。高度透气的微流体芯片作为“气泵”,使得样品的加载和微腔室化可由简单的移液步骤实现,无需额外设备。
为减少热循环周期、缩短检测时间,研究团队利用纳米加工手段,将ZnO纳米棒均匀地积淀在微通道板侧壁。由于纳米棒的表面等离子效应,PCR产物的荧光强度得到了极大增强,DNA扩增终点检测的时间从小时级缩短到25分钟,同时提高了检测精度。此外,该系统的微腔室密度高达1563 mm-2,在指甲盖大小的面积内即可形成超过15万个独立微腔室,这大大提升了dPCR的可扩展性,使得百万级微腔室扩增成为可能。
利用该集成系统,研究人员对噬菌体λDNA和癌症相关PLAU基因进行快速的单分子级别绝对定量。在定量过程中,样本中的目标核酸分子被随机分散在数以万计的独立微腔室中进行扩增。每个微腔室内仅需单个核酸分子即可实现有效扩增,从而被后续的荧光成像和自动化图像分析算法精准识别(图2)。经过反复试验,该技术在核酸绝对定量中的总体测量偏差小于5%。基于上述优势,该新型集成化微系统有望加速数字PCR技术在病原体快速检测、癌症早筛等生物医学领域的广泛应用。
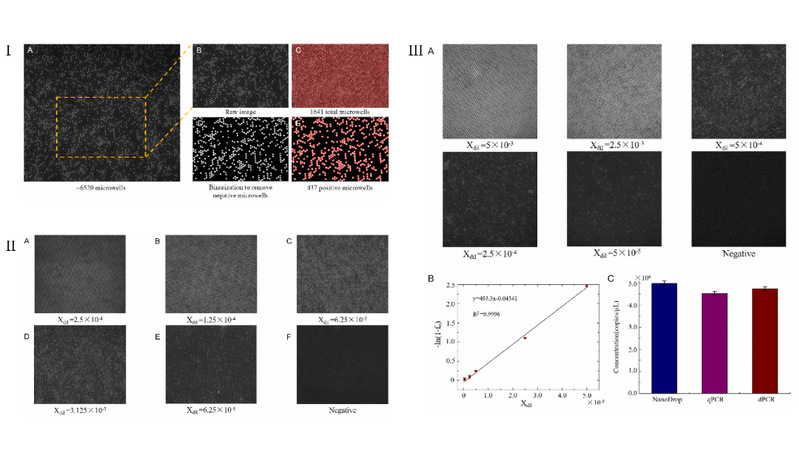
图2 I:从原始图像中识别阳性微孔的数据采集过程,(A)采集热循环后数字PCR芯片原始实验图像,(B)选取目标区域,(C)定位和计数所选微孔,(D)二值化算法去除阴性微孔并增强对比度,(E)标定阳性微孔。II:使用荧光增强数字PCR芯片对噬菌体λDNA进行五步连续稀释并对其进行荧光定量;III:(A)使用荧光增强数字PCR芯片对PLAU基因进行连续稀释并对其进行荧光定量,(B)绘制阳性微孔比例与稀释系数之间的线性回归曲线,(C)荧光增强数字PCR芯片对PLAU基因的定量可与商用的Nanodrop、qRT-PCR相媲美。


